Seriál o detektivní chemii – Příběhy žáru a výbuchů
Detektiv Chemie se rozhlédl po tom, co zbylo z kuchyně.
Nejvíc černé zdi jsou kolem sporáku a hlavně trouby, to se
dalo čekat,
pomyslel si detektiv. Pohled mu zabloudil na
rozsekané okno, kterým sem dopadalo světlo. Ale k oknu nevedla
černá stopa, která by napovídala, že bylo otevřené v době
požáru. Ohořelý byl především pás ve výši očí, což by odpovídalo
hoření plynu. Že by přece jen samovolně chytl plyn z trouby,
který někdo zapomněl zavřít?
Detektiv se opatrně přiblížil ke sporáku a jaké bylo jeho překvapení, když zjistil, že jde o sporák elektrický a v troubě byla plynová bomba.
To mi řekněte, Omáčko, jak někoho může napadnout dát do
elektrické trouby plynovou bombu? Žhář byl buď neuvěřitelně
geniální, nebo naopak neuvěřitelně hloupý…
detektiv
nevěřícně zavrtěl hlavou a šel se poptat majitele, zda jezdí občas
na čundr.
Hóří, hóří…
Říká se, že oheň je dobrý sluha, ale zlý pán. A zlý je i pro pozdější vyšetřování. Stačí si uvědomit, že jako palivo funguje takřka jakýkoliv organický materiál, takže na otisky prstů můžete zapomenout. Mnohdy dokonce zničí celou scénu zločinu, často i vinou pomoci hasičů, kteří se snažili oheň uhasit. Podobně nepříjemně se chovají k důkaznímu materiálu i výbušniny.
Oheň i výbušniny pracují na principu oxidace, jen pravda rozdílnými rychlostmi (viz tabulka 1). Čím vyšší je rychlost oxidace, tím méně stačí přistupovat k reakci kyslík ze vzduchu a je k ní zapotřebí další okysličovadlo.
Hoření je exotermní reakce, která navíc vytváří velké množství plynů. Tím, že produkuje teplo, se plyny ohřívají a expandují. V případě ohně vytvoří plyny sloup dýmu, v případě zbraní tyto plyny rozpohybují projektil a v případě výbušnin vytvoří tlakovou vlnu.
| Typ hoření | plameny, deflagrace | výbuchy, detonace | |
|---|---|---|---|
| Forenzní použití | žhářství, boj s ohněm | střelné zbraně, balistika | letištní kontroly, teroristické útoky |
| Rychlost hoření | subsonická | rychlost zvuku1 | supersonická |
| Palivo2 / typické vazby | hořlaviny C-H, H-H, C=C |
střeliviny C-N |
výbušniny C-O, C=O |
| Okysličovadlo | vzduch, O2 | KNO3, nitrosloučeniny | NO3−, ClO4−, organické peroxidy |
| Vytvářený tlak | nízký | střední | vysoký |
| Typ procesu | termický | mechanický (tlaková vlna) | |
| Příklady | celulóza | střelný prach | TNT, RDX, PETN |
Je důležité si uvědomit, že k hoření jsou zapotřebí tři faktory: palivo, okysličovadlo a teplo (viz obrázek 1). Odstraníte-li alespoň jeden z nich, hoření zastavíte. U paliva a okysličovadla navíc závisí na jejich poměru a u tepla záleží na jeho přenosu.
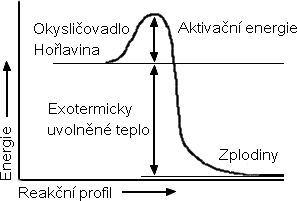
Model hoření dřeva
Nejdřív dochází k pyrolytickému rozkladu dřeva (viz obrázek 2). Tím se z něj uvolní lehčí uhlovodíky, které pak podléhají oxidaci v plameni. Zda bude oxidace úplná (na oxid uhličitý) nebo neúplná (na oxid uhelnatý, případně na saze) rozhoduje teplota plamene a složení hořlavé směsi.
Vliv teploty se mimochodem týká i zachování těl v ohni. Těla se
v ohni poměrně zachovávají. Kremace probíhá zhruba při 800 °C udržovaných po dobu dvou hodin. Oheň
místnosti sice může dosahovat až 1100 °C,
ale většinou jen na příliš krátkou dobu, než shoří jeho palivo. U těl
se nejdřív vypařuje voda, a tak se zkracují svaly až do typického
boxerského
postoje. Ale i zuhelnatělá těla jsou uvnitř poměrně
zachovalá a dá se z nich stále poznat třeba otrava jedem nebo
zranění.
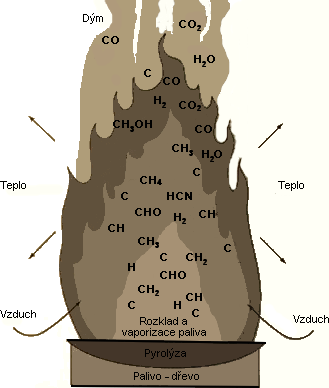
Termodynamika hoření
Aby byla reakce samovolná, musí při ní růst neuspořádanost (entropie) soustavy (ΔS > 0). Tato podmínka je splněna vzhledem k tomu, že při hoření vznikají plyny, které jsou rozhodně méně uspořádaným systémem molekul, než bylo předchozí dřevo. Dalším ukazatelem proveditelnosti reakce je pokles Gibbsovy volné energie G v soustavě (ΔG < 0). Ta je definována pomocí entalpie H (tepla) a entropie S (neuspořádanosti):
Vzhledem k tomu, že se uvolňuje teplo, a to je záporně vzatou entalpií (Q = −ΔH), vidíme, že entalpie klesá (ΔH < 0). Pokud je tedy změna entropie kladná a změna entalpie záporná, znamená to, že záporná bude i změna Gibbsovy volné energie a reakce bude samovolná.
Hoření vyprodukuje jak určitý objem plynů V, tak i teplo Q, a proto se k vyjádření síly hořlavin a speciálně výbušnin používá součin QV. Nejsilnější výbušniny jsou ty, které vyprodukují nejvíce plynů při co nejvyšší teplotě. Nicméně, neměli bychom zapomínat na vliv složení směsi. Nejlépe reakce poběží, pokud bude zajištěna ideální stechiometrie složek směsi, tedy například k hoření 1 molu methanu budeme používat přesně 2 moly kyslíku. Ne vždy tomu tak ale je. Zavedeme si poměr Φ mezi složením směsi a složením ideálním
Hodnota poměru Φ ukazuje, jaké bude spalování směsi3:
- stechiometrická směs (Φ = 1) – ideální směšovací poměr, nejvyšší dosažitelná teplota;
- chudá směs (Φ < 1) – směs je překysličena, teplo se spotřebovává i na ohřev nepoužitého okysličovadla, teplota a tím i účinnost spalování je nižší;
- bohatá směs (Φ > 1) – v systému je nedostatek okysličovadla, spalování je nedokonalé, tepla se uvolní méně.
K hoření navíc dojde jen v případě, že se Φ blíží jedné. Jestliže je v systému příliš mnoho okysličovadla, nebo naopak paliva, k hoření nedojde (viz tabulka 2). Proto taky vybuchují pouze prázdné nádrže s benzínem, a ne nádrže zcela naplněné…
| Látka | Meze [% látky] | Látka | Meze [% látky] |
|---|---|---|---|
| Zemní plyn | 4–15 | Vodík | 4–75 |
| Propan | 2–10 | Acetylen | 2–81 |
| Butan | 2–9 | Amoniak | 16–25 |
Kinetika hoření
Ono se řekne hoření, ale jaký je vlastně jeho mechanismus? Překvapivě složitý. Například u hoření methanu je mechanismus založen na 277 elementárních reakcích, při hoření vzniká 49 meziproduktů. A to jsme vyšli z jednoduché látky, nikoli například z benzínu, který je směsí už na počátku.
Hoření totiž není jednoduché srážení se molekul paliva s molekulami okysličovadla, jak by nás mohlo napadnout ze srážkové teorie. Jde o řetězovou reakci, která je iniciována tvorbou volných radikálů. Ty se posléze propagují srážkami a dalšími rozpady neutrálních molekul. Zanikají až srážkou dvou radikálů. Pokud je rychlost propagace větší než rychlost zániku, tak se reakce šíří.
Přenos tepla
Nejjednodušší model plamene je model adiabatického plamene – ohřívají se pouze produkty reakce. Už tento model nám ukazuje, že při jiném než stechiometrickém poměru je dosažená teplota nižší o ohřev nereagujících částic.
Ale teplo také proudí i jinam – teplý vzduch je lehčí
než vzduch studený, takže značná část tepla odvane
. Oheň také
ohřívá dřevo, které se zplyňuje a tyto zplyněné uhlovodíky oheň dále
živí. Oheň však ohřívá dřevo hlouběji, než kam se dostane kyslík. Zde
dochází k tepelnému rozkladu – pyrolýze –
v reduktivním prostředí. Pyrolýzou vznikají jiné látky než
hořením, a proto vypadá zasažená část jinak než popel po hoření.
No dobře, ale co odlišuje hoření a výbuch?
Rychlost reakce. Nic víc, nic míň. V případě hoření se tvoří odpadní plyny poměrně pomalu a mají dostatek času šířit se do okolí, takže se příliš nezvyšuje tlak.
Naopak u výbuchů se vytvářejí plyny natolik rychle, že je není schopno okolí absorbovat a roste tlak. Mezi místy s rozdílnými tlaky pak vznikne tlaková vlna, která je odpovědná za destrukční účinky výbuchu. Pokud rychlost tlakové vlny nepřesáhne rychlost zvuku v daném prostředí, jedná se o deflagraci. V opačném případě se jedná o detonaci.
Vztah pro rychlost zvuku na vzduchu přibližně popisuje rovnice:
| Typ | Výbušnina | Struktura | Rychlost [m s−1] | Silový index PI – viz (4) |
|---|---|---|---|---|
| Slabá | Azid olovnatý – rozbušky | Pb(N3)2 | 2300 | 14 |
| Silná | Nitroglycerin – dynamit, střelný prach | 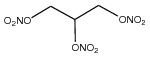 |
7750 | 171 |
| Silná | Kyselina pikrová – standard pro porovnávání explozivního indexu | 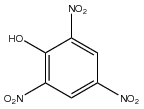 |
7900 | 100 |
| Silná | TNT – oblíbená komerční výbušnina | 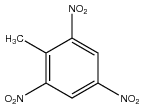 |
6850 | 331,2 |
| Silná | RDX – Hexogen – vojenská trhavina | 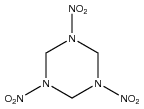 |
8440 | 457 |
Jak jsme už říkali, síla výbušnin je definována podle množství tepla a objemu plynů, které vyprodukují. Relativní sílu pak uvádí rovnice
Poslední skupinou výbušnin jsou střeliviny. Jde povětšinou o homogenní práškové směsi, které mají pomalejší a kontrolovatelnější hoření, než by měly samotné výbušniny, neboť jednolitou strukturou se výbuch šíří rychleji. Pokud by byla rychlost hoření příliš vysoká, hlaveň by explodovala; pokud by byla příliš nízká, náboj by letěl menší rychlostí a tedy i nepřesněji.
První známou střelivinou byl černý střelný prach
starých Číňanů. Jde o směs 15 % uhlíku,
10 % síry a 75 %
ledku (dusičnanu draselného). Jeho nevýhodou byla tvorba černého dýmu,
která nejen že prozrazovala pozici střelce, ale v případě bitvy za
chvíli nikdo nikoho neviděl.4 Číňané samozřejmě
nepoužívali střelný prach jen na ohňostroje, ale také vymýšleli první
palné zbraně. Nejstarší design těchto zbraní byl tzv. ohnivý
oštěp
a šlo vlastně o plamenomet, do kterého se přidaly malé
projektily. Pozdější zbraně pak omezily ohnivou část a připomínaly
spíše brokovnici.
Nevím jak vy, ale rozhodně bych se coby mongolský nájezdník necítil
dobře, kdyby na mě mířil Hromový vrhač ohně s devíti
průraznými magicky otrávenými šípy
.
Koncem 19. století se začaly objevovat bezdýmné střelné prachy, založené většinou na směsi nitrocelulózové želatiny. Recept na bezdýmný střelný prach dále vylepšil Alfred Nobel přidáním nitroglycerinu. A dnes jsou střelné prachy ještě doplněny stabilizátory a hygroskopickými látkami na ochranu před vlhkostí a pojivy.
No dobře, už víte, co a jak hoří, i pár divných výpočtů u výbušnin jste se naučili, zastřílet jste si zastříleli, ale co se vlastně zjišťuje na místě činu?
Zkoumání ohně
U ohně je prvním ukazatelem jeho stopa. Podle ní se dá určit, kde oheň začal (viz obrázek 3). Ze vzhledu místa zdroje ohně se dá určit, zda byl k jeho zapálení použit nějaký urychlovač hoření, ať už plyn (methan), kapalina (benzín) nebo pevná látka (papír). A také by na místě mělo být zápalné zařízení, třeba sirka, zapalovač nebo zkratovaná zásuvka.
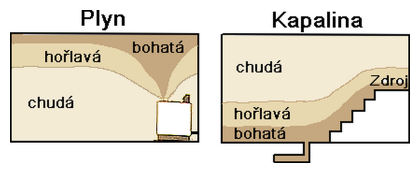
Po plynných urychlovačích hoření sice nezůstanou žádné stopy, ale zůstane po nich nádoba, v které byly na místo přepraveny. Po pevných zůstane aspoň popel, ale nejlépe se analyzují kapalné urychlovače.
Jak je patrné z obrázku 3, kapalina těsně u země nehoří, a tak může zůstat po požáru neshořený urychlovač ukrytý v nějaké škvíře. Proto se sbírají vzorky zbytků po požáru tak, aby se uložily v neprodyšných nádobách s dostatkem volného prostoru.
Kapalná látka bude v rovnováze se svými parami, a tak se prostor nad zbytky nasytí párami urychlovače. Nicméně takto ukryté kapaliny se postupem času z místa činu odpaří, proto je třeba je sesbírat co možná nejrychleji.
Vzorek se poté zkoumá pomocí plynové chromatografie, nejlépe s pomocí hmotnostní spektrometrie jako detektoru (GC-MS). Ten jsme už potkali v druhém dílu seriálu, a tak pokročíme dále.
Zkoumání střelby
Když vypálíme ze zbraně (nemyslím z praku nebo vzduchovky), kromě projektilu z hlavně vyletí zbytky nespálených střelivin, pojiv, podobně jako spaliny a zbytky po rozbušce (obrázek 4). Především rozbuška je vhodným objektem pro zkoumání, díky tomu, že obsahuje těžké kovy, které se posléze dají analyzovat.
Jako rozbuška se nejčastěji používá směs styfnátu olovnatého5, sulfidu antimonitého a dusičnanu barnatého. Nicméně se dnes začínají používat i bezolovnaté rozbušky.


Tyto zbytky se od hlavně šíří kuželovitě do vzdálenosti zhruba 0,5 metru. Jejich složení se mění se vzdáleností – těžší částice doletí dál. Složení se tedy dá použít k určení přibližné vzdálenosti střelce od oběti. A to nejčastěji pomocí mikroskopického vzhledu vzniklých částic Pb-Sb-Ba a také pomocí jejich elementární analýzy. Je navíc nutné tyto ukazatele kombinovat, protože částice obsahující Pb-Sb-Ba se vytvářejí třeba při brzdění auta, ale vypadají trošičku jinak.
Mezi zbytky po výstřelu je možné najít i organické látky, ale ty většinou na místě nevydrží dlouho. Jedná se nejčastěji o zbytky střelivin a zhruba odpovídají složení patrony.
Zkoumání výbušnin
S asi nejčastějším zařízením na testování výbušnin se můžete potkat na letištích. Jsou to oblíbené rámy, kterými se prochází při kontrole zavazadel. Jde o iontovou mobilní spektrometrii (IMS) a kromě detekce výbušnin se používá i k detekci drog.
Sice jsme ji už probírali v druhém dílu seriálu, ale zde se na chvíli zastavíme u typu jednotlivých iontů, jaké v IMS detekujeme.
IMS je založena na elektroforetické separaci iontově-molekulárních shluků podle poměru hmotnosti a náboje. Může se nastavit tak, aby zachytila buď kladné, nebo záporné ionty, přičemž pro detekci výbušnin se nejčastěji používá detekce anionů typu dusičnanů nebo dusitanů.
Z rámu je odebírán vzduch a ten se ionizuje pomocí zářiče 63Ni. Ve vzduchu vzniknou nejčastěji ionty O2−(H2O)n, kde n je počet shluknutých molekul vody. Ty posléze narážejí na jiné molekuly a vznikají pak další fragmenty. Určitý problém představují organické výbušniny, které neobsahují ionty, ale jsou neutrální jako třeba nitroglycerin nebo RDX. Ty se aktivují pomocí iontu Cl−, který se vytváří dopováním vstupního vzduchu o dichlormethan. Vznikají pak shluky M⋅Cl−(H2O)n, jako třeba RDX⋅Cl−(H2O)n a ty už se detekovat dají.
Horší je, že IMS není schopna rozpoznat výbušniny ukryté v tekutinách, neboť netěkají, a tak se dnes do letadla s pitím nedostanete.
Donedávna byla také určitou nevýhodou IMS velikost, ale jako ve většině oborů se snaží výrobci zmenšit zařízení tak, aby byly IMS přenosné, dokonce se uvažuje o velikosti čipu.
Slovo závěrem
Zakončím tento díl zamyšlením nad jedním mýtem držícím se ve forenzních vědách. Lidské tělo se prý může jakýmsi záhadným způsobem samo vznítit a rychle shořet na popel. A to aniž by se plameny nějak zásadně dotkly okolí.
První popsaný případ spontánního uhoření se udál v roce 1662. Jonas Dupot roku 1763 publikoval práci De Incendiis Corporis Humani Spontaneit, ve které vyložil první dvě protikladné teorie o tomto fenoménu:
Podle první teorie předpokládal, že se v těle pohybují
zvláštní látky tzv. humory
. Jejich zrychlený pohyb podle něj
měl analogii v procesech, které v neživotné přírodě vedou
k teplu a ohni.
Podle druhé teorie způsobovalo teplo tření mezi nejmenšími částečkami v krvi a jiných tělních tekutinách v průběhu jejich cirkulace tělem.
Samovznícení se posléze stalo oblíbenou literární metodou, kterou ve svých dílech využili k odstranění postavy i takoví autoři jako třeba Charles Dickens, Honoré de Balzac či Mark Twain. Popisovalo se jako nadpřirozený jev.
K jeho osvětlení potřebujeme odpověď na tři otázky – (1) Byl či nebyl přítomen zdroj tepla? (2) Proč se nic nestávalo okolí? a konečně (3) Jak může člověk jen tak shořet?
Při hledání odpovědi na první otázku se ukázalo, že ve většině případů samovznícení byl ve skutečnosti přítomen i zdroj tepla – nejčastěji cigareta nebo dýmka.
Experimenty se spalováním hovězí a lidské tkáně pak odpověděly na druhou otázku. Prokázaly, že hořením tkáně vzniká tak málo tepla, že oheň se nemůže šířit vně těla. Nemá k tomu dost energie.
Nejdůležitější a nejtěžší otázka ale je otázka, jak může člověk
shořet? Jistě si vzpomenete, co jsem psal o kremaci a poměrně
zachovalých byť zuhelnatělých tělech po požáru. A nejlépe zatím
odpovídá teorie hořícího knotu
, kdy jako knot svíčky
funguje oblečení (nejlépe posypané popelem z cigarety) a takovou
lidskou svíčku pak živí tělesný tuk tak dlouho, dokud není spálena
většina těla a nezůstane jen popel a hromádka kostí.
Lidské tělo se tedy skutečně může vznítit, shořet a netknout při tom své okolí, ale neučiní tak samo.
Skončím seriál o detektivní chemii jasným poselstvím: Kouření škodí zdraví.
Literatura
- Bell, Suzanne. Forensic Chemistry. 1st edition.: Pearson Education, 2006. 614 s. ISBN 0-13-147835-4.
- LYLE, Douglas. Forensics for Dummies. 1st edition.: Wiley Publishing, 2004. 356 s. ISBN 0-7645-5580-4.
- http://en.wikipedia.org – první místo, kam se je většinou vhodné podívat.
- COTE, Artur E., NFPA Fire Protection Handbook, 19th ed.: National Fire Protection Association 2003.
- http://www.nfpa.org
- TURNS, S. R., Introduction to Combustion: Concept and Applications, 2ed.: McGraw-Hill, 2000.
- Christensen, A. M. Experiments in the Combustibility of the Human Body. Journal of Forensic Sciences 2002 (47): 466-470.
- Selvaggi G, Hoste S, Tondu T, Landuyt KV, Hamdi M, Blondeel P & Monstrey S. Spontaneous combustion. J Burns & Surg Wound Care 2003 (1): 14.
- Na vzduchu při 0 °C je rychlost šíření zvuku 330 m s−1.
- Pro přehlednost vynechány anorganické látky jako například Mg, Na, U, Pu…
- Φ je vlastně převrácenou hodnotou λ-faktoru, o kterém jste mohli slyšet u popisu automobilových katalyzátorů. Jde o přebytek kyslíku ve spalovací směsi. Tzv. λ-sonda hlídá složení výfukových plynů a počítač upravuje míchání paliva pro motor tak, aby se snížily emise.
- To byl hlavní důvod, proč byly uniformy v napoleonské době tak jasně barevné.
- 2,4,6-trinitrobenzen-1,3-diolát olovnatý